幹細胞臨床醫學研究
#老年性視網膜黃斑部病變治療 #視網膜色素上皮細胞分化
計畫宗旨與展望
「再生醫學」(Regenerative medicine),是指利用細胞或組織製品,以及具生物可相容性提供細胞生長的生醫材料,經由替換或修復因先天疾病、外傷和老化等所造成之受損人體細胞、組織或器官,來達到恢復或建立正常功能,並有助於患者重獲機能。近年來以幹細胞培養與移植的細胞治療技術領域(Cell Therapy)成為再生醫學的發展主流。再生醫學其中蓬勃發展中,為應用誘導性多功能幹細胞(Induced Pluripotent Stem Cell;iPSC)的細胞治療。日本幹細胞學者山中伸彌(Shinya Yamanaka) 教授於2006年首次在《細胞》期刊上發表將小鼠體細胞重新編譯成為誘導性多能幹細胞(induced pluripotent stem cells; iPSC)的成果,並於2012年獲得諾貝爾生理醫學獎的肯定。日本安倍政府更投注大量資源,發展日本細胞治療技術。2014年理化研究所的高橋政代教授則完成全球首例自體iPSC視網膜幹細胞移植成功之後,也使誘導性多功能幹細胞於再生醫學治療成為因應因全球人口老化以及器官捐贈者不足問題的重要研究方向。過去胚胎幹細胞(embryonic stem cell, ESC細胞)被認為是能力最強的幹細胞,具有分化成多種細胞類型和組織的能力,而成人幹細胞分化的能力較為有限,但是胚胎幹細在倫理與道德上有較大的爭議。誘導型多功能幹細胞可由人體血液或是皮膚中等取得,iPSC細胞不僅沒有胚胎幹細胞的倫理爭議,亦有不易產生排斥等優點。
再生醫療及其誘導多能幹細胞治療的應用包含了用於修復或再生治療型的iPSC與其衍生細胞 (單顆細胞或細胞層片),目前日本有相當多iPSC臨床試驗正在進行:2020年1月27日,日本大阪大學澤芳樹 (Yoshiki Sawa) 教授的研究團隊宣佈,已啟動全球第1例自體iPSC細胞製作的細胞層片「心肌膜」移植到患有重度心臟病患者之心臟的臨床試驗,以確認移植的安全性與療效;另外在2019年8月,西田幸二 (Kohji Nishida) 教授的團隊,宣布利用iPS細胞培養的眼角膜組織,成功移植到1名40歲有嚴重眼角膜疾病之女性患者,且術後並未發生排斥,並且視力也回復到生活所需。 京都大學也在2019年7月提出利用異體iPSC培養軟骨組織,並移植到膝蓋關節軟骨損傷患者,並確認安全及有效性;2018年11月高橋淳 (Jun Takahashi) 教授及其研究團隊宣布,成功將自體iPSC分化的神經細胞移植到50多歲患有帕金森氏症之患者,目前術後良好且正在評估安全性及療效。而高橋政代 (Masayo Takahashi) 博士也在2014年完成第一例自體iPSC分化之視網膜組織治療黃斑部病變;以及2017年有5位患者使用iPSC異體移植治療嚴重眼疾後的結果,5位患者術後狀況皆良好,4位患者視力得以維持,1位有視力有所提升,未發現腫瘤化問題,僅1位發生輕微排斥。
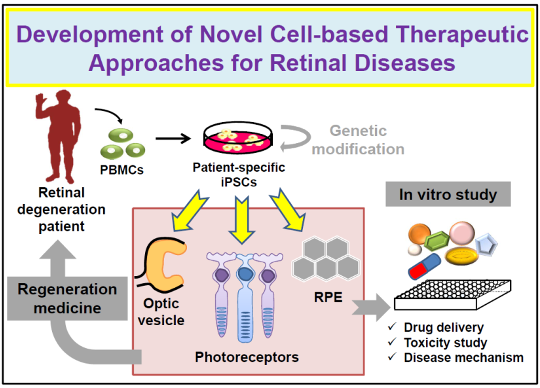
幹細胞治療(包含誘導性多能幹細胞(iPSC)或間質幹細胞(MSC))衍生細胞)在學術和臨床領域表現出很大的希望,但其製成和分化的穩定性仍是個懸而未決的問題。老年性黃斑部病變(AMD)及視網膜疾病已是台灣超高齡社會的疾病之一,所伴隨失能或預後不佳造成社會巨大負擔。本計畫針對視網膜疾病,使用iPSC分化為視網膜色素上皮細胞(RPE)、視網膜神經節細胞(RGC)、三維視泡(3D-OV)以及MSC等。同時,整合校內生醫晶片跨領域研發技術,連結國內半導體設計製造優勢,並與日本山中伸彌教授跨國研發細胞產品之確校平台。製成的臨床等級細胞,可作為細胞移植或再生醫療等商業化之產品。同時,結合臺北榮總臨床研究量能,於2021年衛福部核准iPSC衍生的RPE移植,應用於AMD效果卓越。
本計畫提出四大主軸:
- 生產GTP臨床等級iPSC,將其分化為RPE作為治療AMD使用,並提交第一期臨床試驗。
- 建構GTP等級細胞產品標準操作流程,及其分化為RPE、RGC、3D-OV與MSC。
- 使用半導體生物晶片對細胞產品進行自動化及精準品質管控。
- 開發臺灣純合子iPSC,將其分化為MSC,並推廣為異體細胞治療。本計畫結合臺灣優質臨床研究團隊,及快速、精準、自動化之生物晶片與檢測平台,開發純合子iPSC作為產品大量使用,將可做為推動臺灣生物暨半導體產業發展之關鍵。
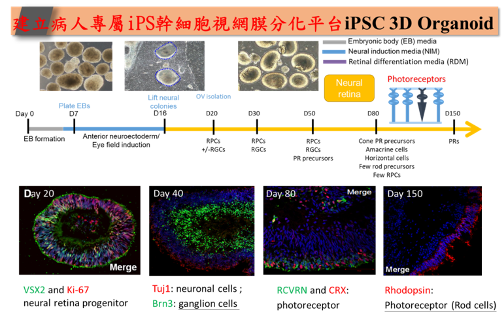
計畫內容
為了達成細胞治療能夠有效的異體化、自動化、量產化之願景,日本2012年諾貝爾獎得主山中伸彌教授所發明之誘導性多能幹細胞(Induced pluripotent stem cell,iPSC)將有效的達成這樣的目標,日本再生醫療國家政策推動重點與細胞治療產品的主流。
因應全球再生醫學細胞治療技術突飛猛進,臨床試驗與細胞產品日趨成熟。本團隊近日於再生醫學與細胞治療量能的突破與提升,未來將繼續配合國家政策以符合衛福部發展重點與國際發展創新醫療的趨勢,持續發展再生醫療技術於臨床應用。本團隊基於iPSC細胞的技術,於本國進行首例iPSC細胞分化視網膜色素上皮細胞移植,愈將iPSC分化視網膜細胞與間質幹細胞應用於視網膜病變(黃斑部病變、視神經病變等)與間質幹細胞應用治療。透過此計畫以下幾點,將臺灣iPSC細胞層面達到更高更廣的臨床應用,本計畫將提出四大主軸:
- 生產GTP臨床移植等級iPSC細胞,將其分化為視網膜上皮細胞作為移植治療黃斑部病變使用,並提交第一期臨床試驗。
- 建構臺灣GTP等級細胞產品一致化標準操作流程,及其分化為視網膜色素上皮細胞(RPE)、視網膜神經節細胞(Retinal ganglion cell; RGC)和三維視泡(3D optic vesicle; 3D-OV)與間質幹細胞(MSC)。
- 建構臺灣iPSC及其分化之細胞,使用半導體生醫晶片進行自動化及精準化品質管控。
- 開發臺灣同合子iPSC細胞,將其分化為間質幹細胞(Mesenchymal stem cell; MSC),並推廣為Allogenic異體移植,例如應用於腹膜纖維化等相關疾病。
基於此四大主軸,具有以下主要目標:
- 生產GTP臨床移植等級iPSC細胞,將其分化為視網膜上皮細胞作為移植治療黃斑部病變使用,並提交第一期臨床試驗。
- 建立源自誘導性多功能幹細胞衍生之移植使用臨床等級視網膜色素上皮細胞、視網膜神經節細胞和三維視泡。
- 建立精準檢測篩選臨床等級具健康活性細胞之生物晶片以建構製程標準化。
- 建立同合子誘導性多功能幹細胞衍生之間質幹細胞應用於腹膜纖維化。
關鍵技術:臨床等級誘導多能幹細胞再生醫療產品開發與臨床試驗平台
一、老年性視網膜黃斑部病變治療
據醫學統計,65歲以上人口中約有十分之一的人口將會罹患「視網膜黃斑部病變」(Aged Macular Degeneration;AMD),「黃斑部」是人類視網膜中央的感光區,佈滿人體最精密的錐狀感光細胞,負責將看到的訊息傳遞至腦部,而老年性黃斑部病變是一種因黃斑部產生病灶導致中心視力衰退的疾病。好發50歲以上的族群,會隨著年齡增長而逐漸退化,是導致老年族群失明的主因。老年性黃斑部病變一般分為乾性(dry type)及濕性(wet type)二種。乾性的老年性黃斑部病變常在黃斑部出現疣性小斑以及色素層病變,病程推展是病灶擴大或更嚴重,使患者視力隨著降低。;濕性老年性黃斑部病變會出現滲水、出血甚至長出新生血管的徵狀,造成視網膜水腫,甚至發生局部剝離狀況,其病程變化快速,症狀惡化時會產生塊狀黑點遮住中心視線,即中心盲點,會在短時間內造成中心視力嚴重受損。黃斑部病變的最新治療方法是使用「眼內注射抗血管新生藥物」,直接作用於不正常的新生血管,可使脈絡膜新生血管萎縮,且結疤較小,病人的視力進步機會較大,是目前治療黃斑部病變的首選,根據2016年美國眼科醫學會期刊的論文研究指出,統計2000年美國整年僅有2922次玻璃體內注射藥物治療,但在2014年暴增到261萬多次玻璃體內注射藥物治療,可見治療此病症的患者與日劇增。目前台灣的治療主要是接受玻璃體內抗血管內皮生長因子(anti-VEGF)注射2年7針的方案;頻繁的玻璃體內注射可能會增加感染、視網膜脫離和晶狀體損傷的風險。此外,大多數視網膜黃斑部病變患者需要終生治療,這對家庭和社會都是巨大的負擔。
二、誘導人類 iPSC 快速高效地向視網膜色素上皮細胞 (RPE) 分化
視網膜色素上皮 (RPE) 細胞對於維持神經視網膜和感光細胞內的正常生理機能至關重要。 RPE 細胞吞噬感光細胞外節的尖端並幫助維持視網膜血管屏障。視網膜的第二個屏障系統是內部視網膜血管屏障(BRB),該屏障由排列在視網膜脈管系統上的內皮細胞組成,而脈管系統起源於視網膜中央動脈並供應視網膜內層。AMD 是全世界視網膜失明的第一大原因,預計發病率將繼續增加。AMD 由於黃斑中的視網膜退化導致中心視力不可逆轉的喪失,黃斑是視網膜中的富含感光細胞的室錐細胞的中央部分[10]。由於 RPE 細胞對於維持下層脈絡膜毛細血管的完整性和阻斷視網膜下新生血管的形成非常重要,因此 RPE 變性和缺損被認為是 AMD 發生和發展的關鍵因素。鑑於治療晚期 AMD 尚無有效治療治療藥物,RPE、感光細胞或其他視網膜細胞的移植是修復 AMD 患者受損視網膜的另一種方法。然而,獲得足夠數量的合適捐贈者 RPE 和感光細胞用於離體移植以挽救 AMD 的視覺功能障礙仍然是這種治療待克服的挑戰。因此,基於多能幹細胞的療法,誘導多能細胞 (iPSC),是再生醫學中有限供體 RPE 的潛在解決方案。
三、亮點績效
(一)邱士華教授研究團隊誘導多能幹細胞之研究成果
邱士華教授之研究團隊利用「人類誘導型幹細胞」(Induced Pluripotent Stem Cell; iPSC)技術,成功將先天性視網膜裂損病人血液細胞轉化成iPSC,進而分化成具病患特有視網膜裂損病徵之「立體視網膜類器官」(3D Retinal Organoid)功能性組織,以模擬人體組織基因突變的缺損模式,進而作為研發新型治療的試驗平台,成果刊登於國際幹細胞知名雜誌Stem Cell Reports (2019 Nov),更可以客製化個人化專屬之iPSC-RPE分化的平台,本研究團隊亦利用了3D類器官技術應用於疾病研究,結合最新奈米醫學科技,充分將iPSC重編程機制技術與奈米醫學做了新的詮釋與應用(ACS Nano 2013; Nanomedicine (Lond) 2014);並以個人化醫療應用於細胞重編程之應用與誘導性多功能幹細胞(iPSC)技術以建立藥物篩選平台與疾病模型,已證實重編程平台於治療退化性疾病(視網膜/視網膜斑退化與其他器官退化等疾病)之應用。邱教授研究團隊以擴大使用分化成細胞產品,佈局用於臨床試驗治療:如經由我們獨有的iPS細胞分化技術,衍生之iPSC-RPE可用於基因型比對成功的患者,本團隊成功採取病患10ml血液成功重新編整為「誘導型多能 (Induced Pluripotent Stem Cell; iPSC)」,並在特定環境中有效率且安全地分化為自體視網膜色素上皮細胞與視神經細胞,透過幹細胞移植以挽救末期黃斑部患者的視力。新式視網膜多功能移植支架系統配合創新開發並建立高純度之視網膜色素上皮細胞分化技術,大幅提升此幹細胞治療的穩定性與提高幹細胞移植之成功率。同時幹細胞只需經過三個代數分化階段步驟,即能提供足夠黃斑部病變患者移植所需之視網膜色素上皮細胞的總量,為黃斑部病變患者的一大福音。

邱教授團隊開發出一種仿生支架,其模仿了具有層粘連蛋白塗層(PDMS-PmL)的血漿修飾聚二甲基矽氧烷片材的視網膜下絨毛基底,為其上生長的RPE單層提供視網膜下環境,並成功開發一種多功能視網膜生物支架系統,並維持RPE細胞分化的穩定微環境(榮獲第12屆生策會國家新創獎學研新創獎-製藥及新醫療技術組第一名&最佳產業效益獎(如下圖)。
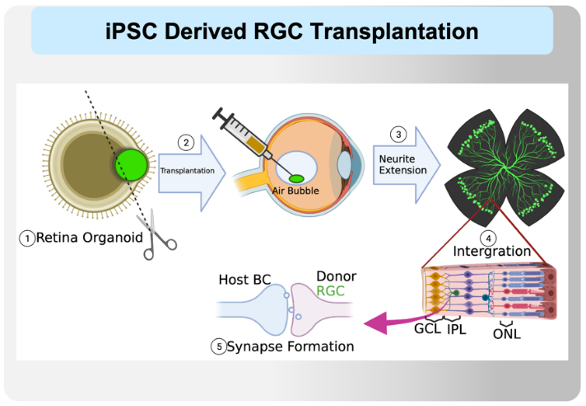
(二)本團隊與日本理研共同研發視網膜神經細胞移植
近幾年日本陸續通過了巴金森症、心肌衰竭、脊椎受損及骨關節的適應症,目前也積極發展血液疾病、糖尿病及肺臟疾病等的治療,再次顯示誘導性多功能幹細胞於再生醫學治療的重要性與臨床價值。日本理化學研究所(RIKEN)的高橋政代教授(Masayo Takahashi)與臺北榮民總醫院和國立陽明交通大學合作。透過幹細胞分化視網膜神經節細胞,移植到視神經病變的小鼠疾病模型的眼球內,移植後的神經細胞不僅順利生長出神經束,並與原先體內的神經細胞產生連結。這個合作成果剛於今110年10月刊登在眼科頂尖研究雜誌IOVS (IOVS. 2021 Oct 4;62(13):26.)。
中樞神經系統 (CNS) 神經的死亡通常是不可逆的,缺乏從疾病或損傷中修復和再生的能力。因此透過移植修補神經是有潛力的治療策略。視網膜被認為是中樞神經系統的一部分,由多種視網膜細胞組成,包括光感受器,作為將光轉換為電信號。另一方面,視網膜神經節細胞 (RGC),透過長的神經束將神經信號傳送到大腦。RGC 的死亡會導致嚴重的視力喪失。青光眼是最常見的眼病之一,其特徵是 RGC 進行性退化和永久性失明,部分原因是高眼壓 (IOP)。為了減緩疾病進展,目前的治療方法通過使用藥物和手術來控制眼壓升高 . 然而,RGCs的喪失是不可逆的,因此需要開發其他治療方法。
在先前的研究中,發表了幾種基於細胞的青光眼和視神經病變療法。例如,骨髓來源的幹細胞、人牙周膜來源的幹細胞和間質幹細胞,是具有神經保護作用,可在RGC 退化的動物模型中防止細胞死亡並促進軸突再生。在這項研究中,我們評估移植的幹細胞衍生的RGC可以與宿主細胞形成細胞連接。根據先前的研究,RGC 分離過程會導致細胞死亡並降低神經活性,因此我們將幹細胞分化為視網膜類器官並手動摘取RGC層。我們的研究結果驗證了RGC 整合的植入策略提供了一種選擇,並為開發用於 RGC 退化的細胞療法提供了可能性。
過去的RGC移植相關研究中顯示,大多數移植後的細胞沒有附著在視網膜上,而是留在玻璃體腔中,這是一個神經營養因子(neurotrophic factors)低的環境。因此,為了促進移植細胞貼附到視網膜,我們使用了液體-氣體交換並吸走了一些玻璃體,將空氣和移植組織注入到玻璃體內,提高移植組織貼附在視網膜表面的效率。在移植後4週後,視網膜免疫染色的結果顯示,移植細胞的存活和神經生長。此外,眼底螢光成像和OCT成像也顯示移植後4週體內的移植細胞持續存活。移植後一周,我們使用鬼筆環肽標記 F-肌動蛋白,顯示在神經突的前緣有生長錐,表示神經有在體內延長跟生長。移植後 12 週 EGFP 陽性沒有顯著變化,並且整個視網膜的截面圖在視網膜IPL 中觀察到神經突(IOVS 2021 OCT)。
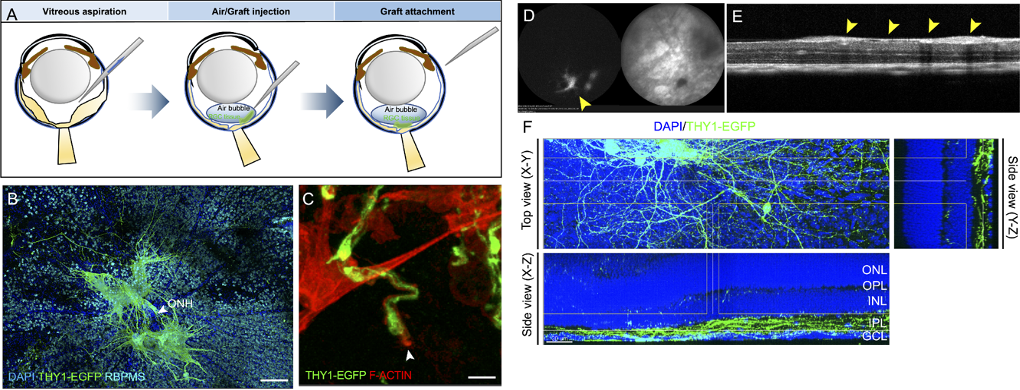
(三)臨床等級誘導多能幹細胞及衍生細胞之研究成果及臨床移植
本團隊將臨床專業知識與重編程相結合,建立臨床級iPSC,並將iPSC分化為iPS&IPSC分化細胞細胞。臨床前研究有iPSC衍生分化細胞的安全性,並進一步於財團法人醫藥品查驗中心諮詢審議;與生技公司的緊密合作將增加生物材料與幹細胞產品。本團隊亦在2019年底利用單細胞核糖核酸定序技術(scRNAseq),利用微流道分離單顆細胞,進而用定序技術來分析增強子在胚胎幹細胞之中調控機制與族群.具有檢體需求量少,可批次檢測大量基因與檢測統計較為顯著等特性.邱教授團隊發現trithorax家族成員Ash2l透過調節增強子中的幾個關鍵事件能有效控制細胞多能性並調節細胞生成,邱教授和他的團隊將Ash21定義為重編程過程中的上調因子。(Nucleic Acids Res.2019 Nov 4; 47(19):10115-10133通訊作者)。
邱教授獲得美國2020年專利.專利中之關鍵技術:利用scRNAseq檢測胚胎幹細胞。
我們團隊發現新轉錄因子Ash2I可調控幹源基因Oct4,因此在Parp1和Ash2l傳遞新機制的發現,不僅是目前幹細胞生物學的劃時代成果,更藉由降低了由正常重編程程序誘導的c-Myc相關致瘤性的發生率,並實質提高了我們誘導多能幹細胞的技術:大為提高本團隊iPSC以及其衍生分化細胞如MSC與RPE的品質與等級。
其他相關子計畫

幹細胞品質監控/產業運用
#細胞斷層掃描 #生醫影像與生醫晶片 #臨床應用且品質穩定的多功能幹細胞 山中伸彌教授2006年發現誘導性多功能幹細胞iPSC(induced pluripotent stem cell)…
臍帶間質幹細胞治療肺纖維化
#首見肺纖維化可逆轉 #已技術轉移並進行臨床試驗 計畫宗旨與展望 當肺部組織受到吸菸、細菌、病毒、空氣汙染、老化、氧化自由基、放射線、化療藥物、或遺傳性等傷害,導致肺泡細胞損傷,使得肺部間質區…
調控間質幹細胞於骨質疏鬆症之治療
#提升間質幹細胞分化效能 #細胞外間質纖維連接蛋白之純化技術 計畫宗旨與展望 骨質疏鬆症是由新骨組織的產生與舊骨組織的破壞之間的不平衡所引起的,是一種影響全世界數百萬人的疾病。目前為止,骨質疏…

以生物科技法律面向/協助政府法規制定
#協助醫事司修法 #解決快速上市之管制爭議與不良反應責任 計畫宗旨與展望 再生醫療具有幾項不同於既有藥物的管制特性: (1)是醫療行為,還是製藥行為?涉及管轄機關和上市規範差異。 (2)快速上市管制爭…
人類誘導型多能幹細胞
#日本京大CiRA基金會 #次世代自動化3D幹細胞培養 計畫宗旨與展望 再生醫學 (Regenerative medicine) 的定義為利用健康的細胞來修復、重組及取代受損細胞功能或組織,讓受傷的細…